[COVID-19의 과학] <2> mRNA와 경구치료제
[※ 본 컨텐츠는 한국화학연구원 제3기 케미러브 서포터즈 활동을 위해 작성된 컨텐츠입니다.]
안녕하세요! 작년 케미러브 서포터즈 2기 활동에 이어서
올해도 또다시 케미러브 서포터즈 3기 활동으로 돌아왔습니다 ㅎㅎ
올해는 한국화학연구원의 최신 연구 성과는 물론이고
화학연구원에서 만든 여러 컨텐츠도 함께 소개해드릴 예정이니까요!
재미있게 봐주시면 감사드리겠습니다!
그럼 시작할게요!

▶ 백신의 세대를 바꾸다 – mRNA 백신

숙주도 바이러스가 자신을 공장처럼 쓰는 것을 지켜만 보고 있지는 않습니다. 특히 인간은 바이러스 뿐만 아니라 다양한 병원체(병을 일으킬 수 있는 외부 물질)의 침입으로부터 몸을 방어하기 위한 아주 정교한 체계를 보유하고 있죠. 바로 ‘면역계’입니다.
인간의 면역 체계는 크게 ‘선천면역’과 ‘후천면역’으로 나뉩니다. 이 둘의 차이는 ‘특이성’, 그리고 ‘기억’이라는 키워드로 설명할 수 있어요. 선천면역은 병원체의 침입이 일어남과 거의 동시에 작동하는 면역 시스템으로, 이미 우리 몸에 만들어져 있거나 만들 준비가 된 자원들을 활용합니다. 이 자원들은 침입한 병원체가 무엇인지를 가리지 않고 무찌르며, 이전에 그 병원체에 노출이 된 적이 있는지와는 무관하게 작동합니다. 반면에 후천면역은 ‘적응면역’이라고도 불리며, 특정한 병원체의 침입에 반응하여 그 병원체를 선택적으로 제거할 수 있는 자원들을 생성하는 방식으로 작동하죠. 이 때문에 후천면역이 병원체에 대응하는 속도는 선천면역에 비해 느린데요. 병원체에 감염이 될 때마다 느리게 반응할 수는 없으니 우리 몸은 병원체를 ‘기억’하는 과정을 추가로 거칩니다. 조금 더 자세히 이야기를 해볼까요? 후천면역이 일어날 때는 T 세포와 B 세포라는 세포들이 활약하는데요. 이 친구들은 선천면역에 의해 몸 안으로 침입한 외부 병원체가 조각이 나면, 그 조각 중 일부를 활용하여 활성화가 되고 병원체와의 전쟁에 동참합니다. 이 과정에서 병원체에 달라붙어 기능을 방해하거나 잡아먹히기 쉬운 형태로 만들어주는 ‘항체(antigen)’가 분비되기도 하고 병원체에 감염된 세포를 터뜨려 죽일 수 있는 물질이 분비되기도 하죠. 그렇게 치열한 전투가 끝나고 나면, 활성화된 T 세포와 B 세포 중 일부는 침입했던 적군에 대한 정보를 기억한 채로 오랜 시간 잠들게 됩니다. 그렇게 잠들었던 ‘기억 세포’들은 후에 똑같은 병원체가 침입하면 깨어나 보다 빠르고 효과적으로 재침입에 대응할 수 있도록 도와줍니다.
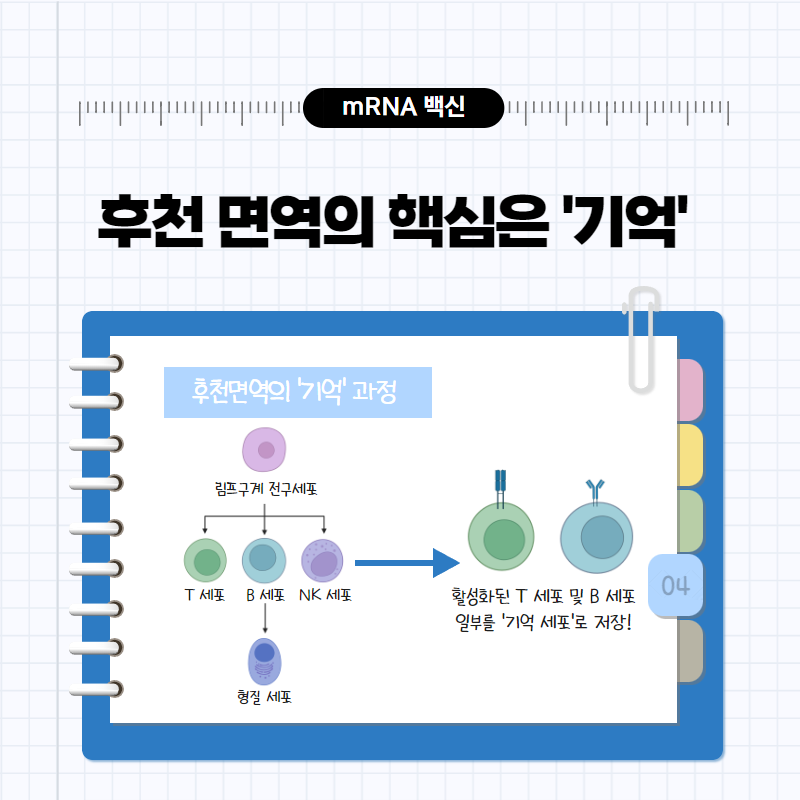
일반적으로 후천면역은 선천면역만으로는 침입한 병원체에 대응하기 어려울 때 작동합니다. 그런데 아직 기억세포가 만들어지지 않은 경우라면 병원체의 침입과 후천면역의 활성화 사이에 시간적인 틈이 생기는데요. 그 틈에 병원체에 의해 선천면역의 방어선이 뚫리고 병원체의 공격에 너무 많이 노출이 되면, 뒤늦게 후천면역이 발동하더라도 이미 건강에 심각한 타격을 입거나 심지어는 사망에 이를 수도 있습니다. 이에 더해 바이러스와 같이 전염성이 높은 병원체의 경우 빠르게 사멸시키지 않으면 어느새 숙주 내에서 복제를 완료하여 또다른 숙주로 옮겨갈 가능성도 있고요. 따라서 사람들은 의도적으로 후천면역의 발동 속도를 빠르게 하는 방법을 고안해내는데, 이것이 바로 ‘백신 예방접종’입니다.
백신 예방접종의 목적은 다시 ‘능동면역’과 ‘수동면역’이라는 두 가지 방식으로 분류가 됩니다. 능동면역을 위한 예방접종에서는 병원체 혹은 그의 일부분을 직접 몸에 주입하는데요. 이를 통해 후천면역 체계를 의도적으로 한 번 활성화하여 병원체에 대한 항체나 기억 세포를 안전하게 형성하도록 유도합니다. 반면 수동면역을 위한 백신은 다른 동물이나 사람으로부터 뽑아낸 항체, 혹은 항체를 만들어낼 수 있는 세포를 투여받는 방식인데요. 능동면역이 모의 전투를 통해 전투 경험을 쌓고 다음 전투에 더 효율적으로 임할 수 있도록 전력을 정비하는 것이라면, 수동면역은 아예 용병을 받아서 임시로 병사의 수 자체를 확 늘려버리는 것입니다.


능동면역을 위한 백신의 역사는 18세기까지 거슬러 올라갑니다. 이 당시 인류를 위협했던 전염병 중에는 ‘마마(媽媽)’라는 속칭으로도 유명했던 ‘천연두(Smallpax)’가 있었습니다. 지금은 영 이름을 들어보기가 힘든 병이지만, 당시만 해도 수많은 사람의 목숨을 앗아간 공포의 대상이었죠. 그런데 영국의 한 마을에서 의사로 활동하던 ‘에드워드 제너(Edward Jenner)’는 이 마을에서 ‘소에 의해 전염되는 약한 버전의 천연두’라고 할 수 있는 ‘우두(Cowpax)’에 걸렸던 사람들이 천연두를 앓지 않는다는 사실을 발견하였죠. 이에 제너는 ‘우두를 앓는 소의 고름의 성분을 뽑아내어 사람에게 주사하면 천연두를 앓지 않는다’는 가설을 세웠고, 여러 차례의 실험을 통해 이를 입증하였습니다. 비록 제너가 그 과학적 원리를 정확히 설명하지는 못했지만, 경험적으로 입증된 ‘종두법’은 세계 각국으로 퍼져나가 수많은 사람을 천연두로부터 구해내었습니다. 19세기 중반에는 ‘생물속생설’을 주창한, 한국에서는 모 대기업의 우유 브랜드로 유명한 위대한 생물학자 루이 파스퇴르(Louis Pasteur) 역시 가축을 대상으로 탄저병에 대한 능동면역을 형성하는 백신과 사람을 대상으로 광견병에 대한 능동면역을 형성하는 백신 예방접종을 연구한 것으로 유명하죠.
한편 수동면역을 형성하는 백신은 19세기 후반 독일의 생리학자 에밀 아돌프 폰 베링(Emil Adolf von Behring)과 일본의 의학자 기타사토 시바사부로(Kitasato Shibasaburo)에 의해 최초로 개발되었는데요. 이들은 각각 디프테리아와 파상풍의 치료법을 연구하던 중 서로 협업을 진행하여 이 병에 걸린 동물의 혈액으로부터 분리해낸 ‘혈청’을 주사하면 면역이 형성됨을 발견하였습니다. 이러한 공로로 베링은 1901년 최초의 노벨생리학·의학상을 수여 받기도 하였죠.
수많은 질병들에 대한 예방접종이 연구된 현재에는 수동면역을 위한 백신은 약화된 병원체를 주입하는 것조차도 위험하거나 병원체가 주입되더라도 스스로 후천면역을 형성할 수 없는 사람들, 혹은 능동면역을 위한 예방접종을 받기 전에 병원체에 감염된 사람들에게 주로 시행됩니다. 반대로 이야기하면, 병에 걸리기 전에 미리 ‘예방’을 하기 위해 맞는 주사의 대부분은 능동면역의 형성을 위한 백신이라는 것이죠.

2022년 현재 COVID-19 에 대응하기 위한 정말 다양한 종류의 백신이 개발되었습니다. 한국화학연구원 역시도 백신 개발을 위한 연구에 열심히 참여하였는데요. 2021년에는 '신종바이러스융합연구단(CEVI)' 에서 신규 백신 후보 물질 'IN-B009'를 개발하여 국내 기업과 기술이전협약을 맺고 제1상 임상 시험 역시 진행하였습니다. IN-B009 는 바이러스의 유전자 중에서 스파이크 단백질 (이 단백질에 대해서는 아래에서 더 자세하게 설명할 예정입니다!) 부분을 암호화하는 서열을 뽑아낸 후, 이를 다른 미생물의 유전자에 재조합하여 해당 미생물이 스파이크 단백질을 잔뜩 재생산하도록 하는 '재조합 단백질'을 이용한 백신인데요. 스파이크 단백질을 주입함으로서 우리 몸이 바이러스에 대항할 항체를 생성하고 면역력을 갖추게 되는 시스템이라고 생각하시면 이해가 편하 것 같습니다!
한편 전세계적으로 가장 유명하고 또 가장 뜨거운 이슈인 COVID-19 백신 역시도 능동면역을 형성하도록 유도하는 백신입니다. 그런데 이 백신은 여태까지의 백신과는 조금 다른 특별한 유형의 백신인데요. COVID-19에 관심이 많으신 분들이라면 한 번쯤은 들어보셨을 그 용어, 바로 ‘mRNA 백신’입니다.

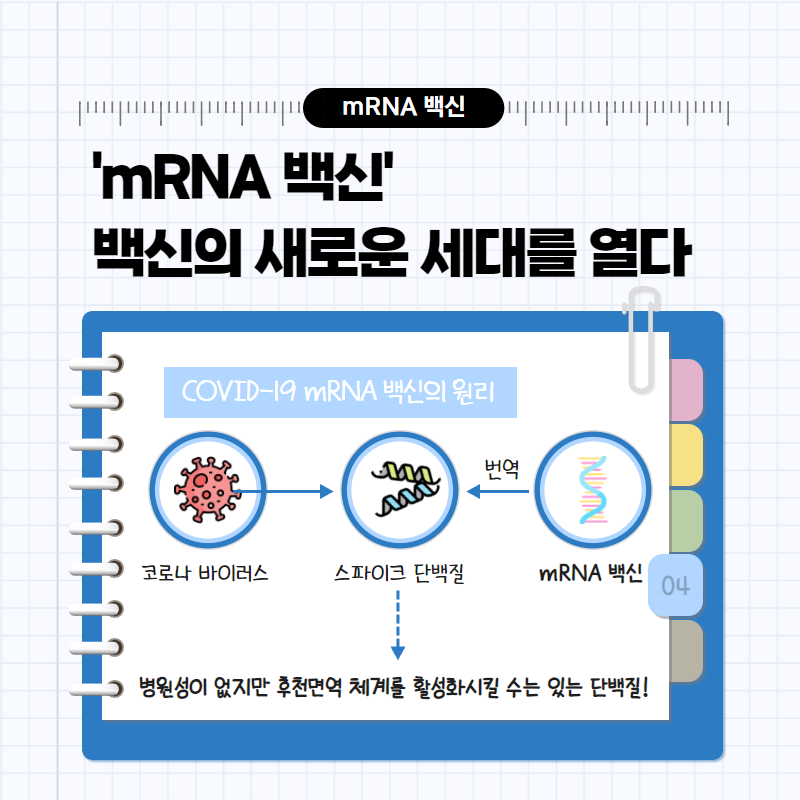
백신의 다음 세대를 열었다고도 평가받는 mRNA 백신은 도대체 무엇일까요? 앞서 설명하였듯 기존의 능동면역을 위한 백신은 병원체인 바이러스 자체를 투입하는 방식을 주로 사용하였습니다. 단지 투입하는 바이러스를 힘을 약화시키거나 아예 기능을 정지시켜버려 단백질과 핵산을 섞어놓은 덩어리에 불과하도록 만들었을 뿐이죠. 전자의 경우를 ‘약독화백신’ 혹은 ‘생(生)백신’이라고 부르고, 후자의 경우를 ‘불활성화백신’ 혹은 ‘사(死)백신’이라고 부릅니다. 앞서 제가 능동면역을 형성하는 과정을 병원체에 대응하기 위한 모의 전투 과정으로 비유하였죠? 완벽히 들어맞는 비유는 아니지만 생백신 접종은 적군의 병사로 분장한 아군 병사들과 대련이라면, 사백신 접종은 적군의 병사처럼 꾸민 목각인형과의 대련이라고 생각하시면 이해가 쉬우실 것 같습니다.
한편, mRNA 백신은 바이러스 전체가 아니라 이름 그대로 mRNA 조각이 담겨 있는 백신인데요. mRNA가 DNA의 전사 과정에서 만들어지는 핵산 가닥이고, 번역 과정에서 만들어질 폴리펩타이드 사슬에 대한 정보를 가지고 있는 물질이라는 것은 중심원리에 대해 설명한 문단에서 이미 언급을 했었죠? mRNA 백신에 들어가는 mRNA는 본래의 SARS-Cov-2 바이러스를 구성하는 일부분인 ‘스파이크 단백질(Spike Protein)’에 대한 정보를 암호화하고 있습니다. 따라서 이 mRNA가 우리 몸 안에 들어오면, 바이러스의 (+)-sgRNA의 번역이 일어나듯이 세포 내의 리보솜에서 이 mRNA의 번역이 일어납니다. 그 결과 스파이크 단백질 조각의 대량 생산이 일어나죠. 그런데 이 스파이크 단백질 조각 자체는 다른 사람에게 전염이 되지도 않고, 그렇다고 체내에서 마구 증식을 일으켜서 COVID-19를 발병시킬 능력을 가지고 있지도 않습니다. 하지만 우리의 몸은 ‘어? 못 보던 녀석인데? 일단은 제거하고 기억도 해둬야 하겠는걸?’이라는 후천면역 반응을 일으키는데요. 그 결과 나중에 ‘진짜’ SARS-Cov-2 바이러스가 침입했을 때 스파이크 단백질 부분에 대한 기억세포가 활동을 시작하면서, 이 바이러스 전체에 대한 보다 빠른 후천면역 시스템이 작동할 수 있게 됩니다. 즉, mRNA 백신 접종은, 적군으로 분장한 병사나 목각인형이 아니라 적군의 무기나 병사에 대한 정보를 담은 문서를 바탕으로 시뮬레이션을 진행하는 것이라고 생각하시면 편할 것 같습니다.
mRNA 백신은 연구가 시작된 지도 얼마 안 되었을뿐더러 2020년 COVID-19에 대응하기 위해 화이자 사(社)가 개발한, ‘화이자 백신’이라는 이름으로 더 많이 불리는 ‘BNT162b2 백신’이 인간에게 사용되는 것이 승인된 최초의 사례일 정도로 역사가 짧습니다. 유전 물질에 대한 인간의 이해도가 점차 높아지기 시작한 시점 자체가 20세기 중반일뿐더러, 바이러스가 어떤 DNA 혹은 RNA 서열을 가지고 있고 그것이 어떤 정보를 담고 있는지를 파악하기 위한 분석 기법은 20세기 후반에야 비로소 상용화되었거든요. 거기에 더해서 백신으로 활용하기에 적합한 서열의 RNA를 디자인하여 공장에서 대량 제조하고, 제조된 mRNA 백신이 운송이나 보관 과정에서 변성되지 않고 접종을 받은 사람의 몸 안에서 무사히 번역이 이루어질 수 있도록 보호하는 데에는 2022년 현재를 기준으로도 최첨단의 유전학 및 나노과학 지식과 기술이 필요합니다. 그러니 정말로 mRNA 백신이 ‘차세대 백신’, 혹은 ‘현대 과학계의 총아(寵兒)’라고 불리는 것이 과장은 아닌 셈이죠.
▶ ‘코시국’의 게임 체인저, 경구용 치료제?

mRNA 백신을 포함한 다양한 SARS-Cov-2 바이러스의 백신은 분명 COVID-19 감염자가 폭발적으로 증가하는 것을 억제하고, 설사 바이러스에 노출이 되더라도 심각한 질환으로 이어지지 않는 데에 도움을 줍니다. 하지만 백신이 COVID-19의 ‘치료제’인 것은 아닙니다. 위의 설명을 읽어보셨으면 알겠지만, 백신은 우리 몸이 바이러스의 침입에 더 잘 대응할 수 있도록 해주는 약물일 뿐 바이러스를 직접적으로 제거하는 효능을 가진 약물이 아니기 때문이죠.
‘코시국’. 본래는 한 인터넷 커뮤니티에서 ‘이 시국에’라는 말 대신 쓰던 ‘밈’이었지만, 현재는 ‘COVID-19’의 첫 글자와 ‘시국’이라는 글자를 합쳐, 팬데믹으로 인해 마스크 착용, 사회적 거리 두기 등이 일상화된 요즘의 시대를 부정적으로 바라보는 용어로 널리 활용되고 있습니다. ‘코시국’에 접어든지 2년이 되어가던 2021년 말, 꽤나 반가운 소식들이 연이어 전해집니다. 소위 ‘알약’이라고 불리는, 입으로 투여할 수 있는 경구 치료제가 개발되었다는 것이죠. 경구 치료제는 주사제와는 달리 휴대가 간편하고 일상생활을 하면서도 복용할 수 있다는 장점이 있는데요. 이 때문에 화이자 사의 최고 경영인 앨버트 불라(Albert Bourla)는 자신들이 개발한 경구 치료제가 기나긴 ‘코시국’을 종식시킬 진정한 ‘게임 체인저’라고 자평하기도 하였습니다.
현재 가장 많은 관심을 받고 있고 실제 발병 환자들에게 투여되고 있는 대표적인 경구 치료제는 두 가지입니다. 하나는 독일의 초거대 화학 기업인 머크 그룹에서 개발한 ‘몰누피나비르(Molnupinavir)’이고, 또 하나는 RNA 백신의 상용화를 최초로 이루어 낸 화이자 사(社)가 개발한 ‘팍스로비드™(Paxlovid™)’입니다. 그런데 이 두 약물이 SARS-Cov-2 바이러스가 우리 몸 안에서 활개를 치지 못하도록 막는 방법은 사뭇 다릅니다.
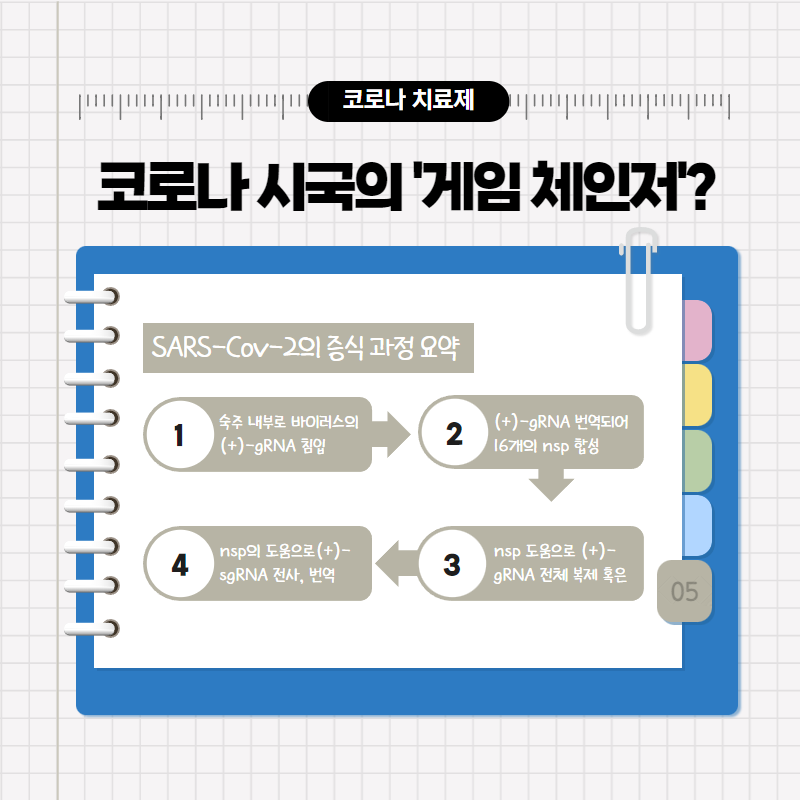
이 두 치료제들이 어떤 원리로 작용하는지를 알아보기 전에, 우선 SARS-Cov-2 바이러스가 어떻게 숙주의 몸 안에서 증식하는지를 다시 한 번 간략히 정리해볼까요?
① 숙주의 몸에 자신의 (+)-gRNA를 집어넣습니다.
② 그 중 일부 서열을 숙주 세포의 도움으로 번역하여 16개의 nsp 단백질을 합성합니다.
③ 그 단백질들의 도움으로 (+)-gRNA 전체를 복제하거나
④ (+)-gRNA 서열의 일부분인 (+)-sgRNA를 전사하고 숙주 세포의 리보솜을 이용해 번역합니다.
바이러스가 성공적으로(?) 증식을 하기 위해서는 사실 이 모든 과정이 문제없이 이루어져야 합니다. 반대로 이야기하면, 이 네 단계 중 하나의 단계에라도 제동이 걸린다면, 바이러스는 정상적으로 증식할 수 없다는 것이죠. 이것이 바로 지금부터 이야기할 두 치료제가 SARS-Cov-2를 억제하는 원리입니다.
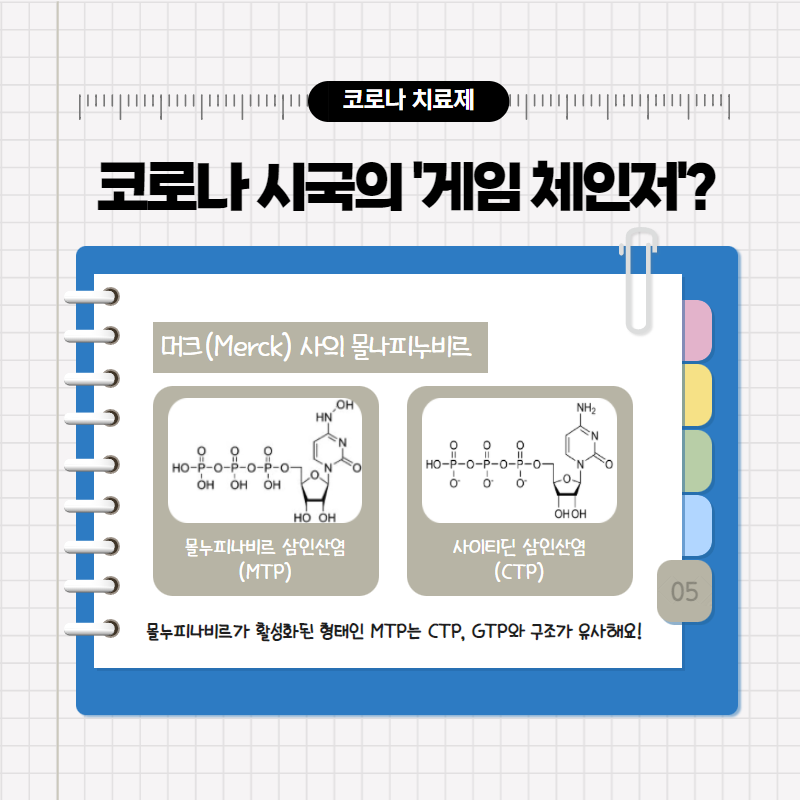

몰누피나비르는 위 네 단계 중 ③번 과정, 즉 바이러스의 (+)-gRNA가 복제되는 과정이 제대로 일어나지 못하도록 방해합니다. 몰누피나비르가 우리 몸 안에 들어오면, RNA를 구성하는 단량체인 뉴클레오타이드와 매우 유사한 구조를 가지는 ‘몰누피나비르-삼인산염(MTP)’라는 물질로 활성화됩니다.
이 MTP는 RNA-의존 RNA 중합효소에 의해 바이러스의 (+)-gRNA를 주형 가닥으로 (-)-gRNA를 전사하는 과정에서 C나 U가 포함된 뉴클레오타이드가 들어가야 할 자리에 대신 끼어들어, 변형 (-)-gRNA 가닥을 합성하도록 유도합니다. 이렇게 합성된 변형 (-)-gRNA는 다시 주형 가닥으로 쓰여 전사가 일어나는데요. 이 과정에서 결과적으로 본래의 (+)-gRNA 가 아닌 돌연변이가 일어난 염기 서열이 합성이 되고, 잘못된 유전 물질을 지속적으로 복제하게 된 바이러스는 결국 증식을 하지 못하고 소멸하게 됩니다. 조금 어렵게 느껴지실 수도 있는데, 앞선 포스팅에서 제가 바이러스의 유전 물질 복제 과정이 중세 시대에 목판을 만들어 책을 찍어내는 과정과 비슷하다는 말씀을 드렸던 것을 기억하시나요? 비유하자면 몰누피나비르는 ‘바이러스의 유전 정보’라는 책의 목판이 만들어지는 과정에 끼어들어 목판의 내용이 원본과 달라지게 하고, 그렇게 만들어진 목판을 이용해 내용이 달라진 책을 계속 찍어내는 작업을 유도한다고 할 수 있습니다.
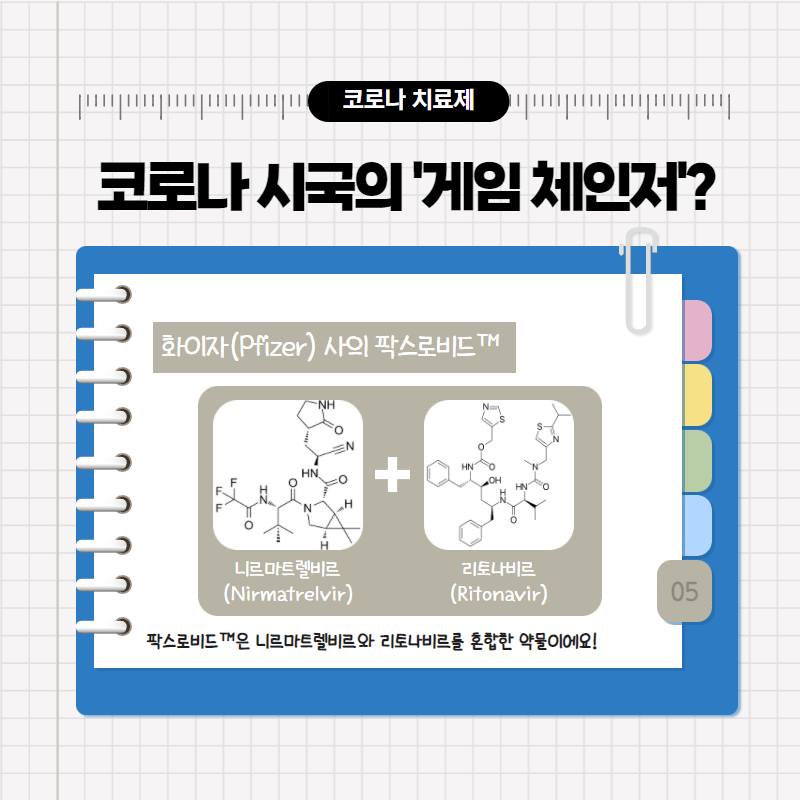
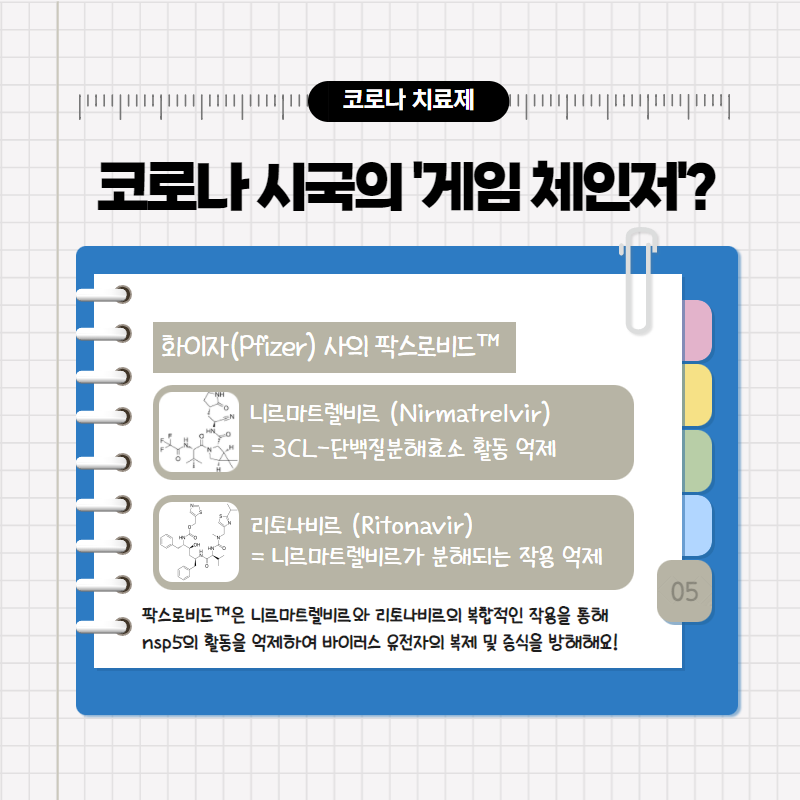
반면 팍스로비드™은 위의 네 과정에서 ②번 과정을 방해하는 약물입니다. 사실 팍스로비드™은 ‘니르마트렐비르(Nirmatrelvir)’ 라는 물질과 ‘리토나비르(ritonavir)’라는 물질로 이루어져 있는데요. 이 중에서 실질적으로 ②번 과정을 방해하는 데에 쓰이는 물질은 니르마트렐비르입니다.
앞선 포스팅에서 바이러스의 (+)-gRNA 중 ORF1 부분이 번역되면 길이가 아주 긴 하나의 폴리펩타이드 사슬이 만들어지고, 이것이 수선을 거쳐 16개의 nsp 단백질이 형성된다고 이야기를 드렸었죠? 이 과정을 조금 더 자세히 들여다보면, 우선 긴 폴리펩타이드 사슬로부터 ‘nsp5’라는 nsp 단백질이 먼저 잘려 나오고, 이 ‘nsp5’ 단백질이 또다시 폴리펩타이드 사슬을 자르는 가위로 작용하여 ‘nsp12’를 포함한 12개의 nsp 단백질들을 추가로 만들어냅니다. 이처럼 단백질임에도 폴리펩타이드 사슬을 자르는 기능을 하는 효소를 ‘단백질분해효소(protease)’라고 부르는데요. nsp5는 프로테이스 중에서도 ‘3CL-단백질분해효소’로 분류되는 단백질입니다.

그리고 니르마트렐비르는 이러한 3CL-단백질분해효소에 달라붙어, 이 효소가 가위질을 하지 못하도록 억제하는 효과를 가집니다. 즉, 니르마트렐비르가 투여되면 nsp5의 활동이 억제되면서 ③번과 ④번 과정에 필수적인 nsp12를 비롯한 다양한 nsp 단백질들이 합성되지 못하고, 이로 인해 바이러스의 증식이 억제되는 것입니다. 앞서 몰누피나비르가 엉뚱한 목판을 만드는 데에 관여한다고 말씀을 드렸었는데요. 팍스로비드™는 아예 목판을 만들지 못하도록 조각칼을 압수하거나, 혹은 만들어진 목판을 책으로 찍어내지 못하도록 먹물을 압수하는 것과 같은 효과를 내는 약물이라고 할 수 있겠습니다.
잠시만요. 그렇다면 도대체 리토나비르는 이 약에 왜 섞여 있는 걸까요? 사실 니르마트렐비르가 제대로 작용하기 위해서는 항상 체내에서 일정 농도 이상을 유지하여야 하는데요. 문제는 이 물질이 체내에서 분해가 이루어집니다. 즉, 니르마트렐비르만을 복용하면 체내에서 이 물질의 농도가 꾸준히 감소한다는 것이죠. 따라서 니르마트렐비르의 분해도 어느 정도는 억제를 해줄 필요가 있는데, 그 역할을 해주는 물질이 바로 리토나비르인 것입니다.
▶ 완벽한 승리는 가능할까?

바이러스는 인류보다도 먼저 이 지구에 나타난 것으로 추정되며, 인류의 역사가 기록된 이래로 항상 함께 해온 존재입니다. 그리고 인류의 역사가 기록된 이래로 대부분의 시기 동안 인간은 바이러스가 몰고 온 질병 앞에 번번이 무릎 꿇고는 했었죠. 초자연적 존재의 변덕으로밖에 보이지 않았던 역병 앞에 사람들은 공포에 떨어야만 했습니다.
그러나 과학과 공학의 발전은 점차 인류가 전염병에 대응할 수 있는 힘을 길러주었습니다. 역병의 창궐이 초자연적인 재앙이 아니라 생물, 혹은 생물 같은 무언가에 의한 것임을 깨닫게 해주었고, 그에 따라 병세를 완화하거나 원인을 제거할 수 있는 약물이 개발되었습니다. 도시의 위생이 개선되어 병원체가 들끓기 어려워졌고, 식량 생산량의 폭발적인 증가로 인류의 영양 상태가 전반적으로 개선되었죠. 그리하여 실제로 인류는 지구에서 전염병 하나를 완벽히 뿌리 뽑는 데에 성공하기도 했습니다. 앞서 백신에 대해 설명할 때 언급된, 최초의 능동면역 백신이 개발되었던 질병인 ‘천연두’입니다. 세계보건기구는 1980년 5월 공식적으로 천연두가 ‘자연적으로’ 발병할 가능성이 더 이상 없음을 선포하였는데요. 그 이후로 현재까지 대한민국에서는 천연두의 발병은 물론 천연두에 대한 예방접종마저도 중단된 상태입니다.
이처럼 과학기술의 힘으로 바이러스에 의한 질병으로부터 승리한 경험이 있으니, 우리가 COVID-19 와의 전쟁에서도 완전한 승리를 거둘 수 있으리라는 희망을 가져도 괜찮을까요? 사실 낙관하기는 힘듭니다. 사람을 대상으로 하는 바이러스에 의한 전염병 중 박멸이 된 질병은 위에서 언급한 천연두가 ‘유일’하거든요. 동물을 대상으로 한 질병으로 범위를 넓혀보아도 천연두를 제외하면 공식적으로 박멸이 선언된 바이러스는 우역바이러스 뿐입니다.
가장 큰 문제는 바이러스의 유전물질에 돌연변이가 일어나기 너무 쉽다는 것입니다. 특히 RNA를 유전물질로 활용하는 바이러스는 더더욱 변이가 잘 일어나죠. RNA 의존-RNA 중합효소를 활용하여 RNA를 복제할 경우, 복제 과정에서 오류가 일어날 확률이 커지고 이 오류가 바로잡힐 가능성도 적기 때문입니다. 아니, 몰누피라비르 이야기를 할 때는 오류가 생기면 증식이 불가능해져서 바이러스를 제거할 수 있다더니, 갑자기 돌연변이 때문에 박멸이 힘들어진다니 이게 무슨 소리일까요?
인간이 바이러스에 대항하기 위해 자체적인 면역 시스템은 물론이고 치료제나 백신, 소독제 등을 활용하면, 바이러스도 가만히 당하고 있지만은 않습니다. 인간이 만들어낸 무기로부터 살아남기 위해 자신의 유전 물질에 의도적으로 돌연변이를 일으켜 약물에 저항할 수 있는 능력을 만들거든요. 심지어 인간이 별다른 일을 하지 않아도, 보다 많은 숙주들에게 퍼져나가기에 유리한 특성을 가진 돌연변이는 마지막까지 살아남아 위세를 떨치거든요. 요즘 뉴스를 보면 ‘오미크론 변이’가 일어난 버전의 SARS-Cov-2 바이러스가 본래의 바이러스와 ‘델타 변이’가 일어난 바이러스를 밀어내고 ‘우점종’이 되고 있고, 이런 변이가 일어난 바이러스는 백신의 효력이 떨어질 수도 있다는 기사를 종종 보셨을텐데요. 요즘의 상황이 바로 바이러스의 유전 물질의 돌연변이를 통해 약물에 대한 내성을 갖추고 보다 강력한 전파력을 갖추는 사례를 잘 보여주고 있습니다.
물론 인류에게 가장 좋은 시나리오는 SARS-Cov-2 바이러스의 완전 박멸에 따른 COVID-19의 완벽한 종식이겠죠. 하지만 그것만이 유일한 시나리오는 아닐 수도 있습니다. 우리가 일상에서 가볍게만 생각하는 감기 역시도 사실은 바이러스에 의한 감염증입니다. 관여하는 바이러스도 워낙 다양하고 심지어 각각의 바이러스도 돌연변이가 워낙 자주 일어나 치료제는 고사하고 백신도 만들어지지 않은 감염병이죠. 그저 충분한 휴식을 취하며 증세를 완화하는 약물을 먹으면서, 우리 몸의 면역계가 바이러스를 제압할 때까지 기다리는 것이 능사일 뿐입니다. 그럼에도 불구하고 대부분의 사람들이 감기에 걸리는 것을 무서워하지 않는 것은, 그만큼 감기 바이러스의 독성이 약화되어 건강 상의 심각한 문제를 일으키지 않는 경우가 많기 때문입니다.
COVID-19의 미래는 무엇이 될까요? 제2의 감기일까요? 아니면 제2의 천연두일까요? 그것도 아니면 제1의 COVID-19로 인류 질병사의 또 다른 별종으로 남게 될까요? 확실한 것은 COVID-19는 이미 ‘단순한 독감’ 정도로 치부하기엔 인류에게 너무도 많은 상처를 남겼다는 것입니다. 부디 내년 이맘 때에는 “COVID-19는 인류에게 큰 피해를 입‘혔’던 질병이다”라고 과거형으로 말할 수 있는 날이 오기를 바랍니다.
[그림 출처]


[참고 자료]
- 천진우, "[코로나19 과학 리포트 2]_Vol. 15 모더나의 백신 개발 팀사이언스(team science)의 힘", 기초과학연구원, 2021년 6월 21일 발행, https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000001003/selectBoardArticle.do?nttId=20080&pageIndex=1&searchCnd=&searchWrd=
- 고규영, 강석, "[코로나19 과학 리포트 2]_Vol. 4 백신의 종류와 특징", 기초과학연구원, 2021년 1월 22일 발행, https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000001003/selectBoardArticle.do?nttId=19594
- 이성규, "세계 최초 노벨 생리의학상 수상자", 사이언스타임즈, 2018년 11월 20일 발행,
- Savoy, M. L., "예방접종의 개요", MSD 매뉴얼, 2020년 10월 8일 수정. https://www.msdmanuals.com/ko-kr/%ED%99%88/%EA%B0%90%EC%97%BC/%EC%98%88%EB%B0%A9%EC%A0%91%EC%A2%85/%EC%98%88%EB%B0%A9%EC%A0%91%EC%A2%85%EC%9D%98-%EA%B0%9C%EC%9A%94
- 김은영, "백신으로 인류를 구하다", 사이언스타임즈, 2021년 3월 22일 발행, https://www.sciencetimes.co.kr/news/%EB%B0%B1%EC%8B%A0%EC%9C%BC%EB%A1%9C-%EC%9D%B8%EB%A5%98%EB%A5%BC-%EA%B5%AC%ED%95%98%EB%8B%A4/
- NCRID 바이러스성 질병 부서, "mRNA COVID-19 백신 이해하기", CDC, 2022년 1월 4일 수정, https://korean.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccines/mRNA.html
- IBS, "질병으로부터 건강을 지켜주는 백혈구 어벤저스", 기초과학연구원, 2021년 4월 14일 수정, https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000000901/selectBoardArticle.do?nttId=15230&pageIndex=1&mno=sitemap_02&searchCnd=&searchWrd=
- 김빛내리, "[코로나19 과학 리포트 2]_Vol. 14 IBS가 밝혀낸 코로나19 유전자 지도의 의미", 기초과학연구원, 2020년 4월 29일 발행,
https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000000971/selectBoardArticle.do?nttId=18475
- Sola et al., "Continuous and Discontinuous RNA Synthesis in Coronaviruses", Ann. Rev. Virol, 2(1) (2015): 265-288, DOI: 10.1146/annurev-virology-100114-055218
- Hillis, D. M. et. al. Principles of Life (first edition), W. H. Freeman & Co.: VA, 161-162, 245 (2010)
- Stryer, L. et. al. 저, 박인원 et. al. 역, Stryer 생화학 (8판), 범문에듀케이션: 서울, 75-76, 123, 146, 149-150, 172, 880-882 (2016)
- Crick, F. "Central Dogma of Molecular Biology", Nature 227(8) (1970): 561-563
- Diana Kwon, "The Promise of mRNA Vaccines", TheScientist, 2020년 11월 25일 수정
- 남대열, "mRNA 백신은 하루 아침에 뚝딱 나오지 않았다", 히트뉴스, 2021년 10월 16일 수정, http://www.hitnews.co.kr/news/articleView.html?idxno=36416
- Jimenez, D. "Paxlovid: what we know about Pfizer’s Covid-19 pill", Pharmaceutical Technology, 2022년 1월 20일 수정, https://www.pharmaceutical-technology.com/features/paxlovid-pfizer-covid-19-pill/
- Mahase, E. "Covid-19: Pfizer’s paxlovid is 89% effective in patients at risk of serious illness, company reports", BMJ 375 (2021): n2713, DOI : https://doi.org/10.1136/bmj.n2713
- Pfizer Inc. "Pfizer’s Novel COVID-19 Oral Antiviral Treatment Candidate Reduced Risk of Hospitalization or Death by 89% in Interim Analysis of Phase 2/3 EPIC-HR Study", Pfizer, 2021년 11월 5일 수정, https://www.pfizer.com/news/press-release/press-release-detail/pfizers-novel-covid-19-oral-antiviral-treatment-candidate
- Rut, W. et. al. "Substrate specificity profiling of SARS-CoV-2 main protease enables design of activity-based probes for patient-sample imaging", bioRxiv (2020), DOI : https://doi.org/10.1101/2020.03.07.981928
- Kabinger, F. et. al. "Mechanism of molnupiravir-induced SARS-CoV-2 mutagenesis", Nature Structural & Molecular Biology 28 (2021): 740–746.
- NIH, "The COVID-19 Treatment Guidelines Panel's Statement on Potential Drug-Drug Interactions Between Ritonavir-Boosted Nirmatrelvir (Paxlovid) and Concomitant Medications", NIH, 2021년 12월 30일 수정, https://www.covid19treatmentguidelines.nih.gov/therapies/statement-on-paxlovid-drug-drug-interactions/
- 김양원, "[팩트체크] "코로나19는 이제 감기 수준 아닌가?", YTN, 2021년 9월 13일 수정, https://www.ytn.co.kr/_ln/0105_202109130903257112





