[10월] 비누와 세척제의 원리
환절기가 되면 위생 관리를 위해 손씻기가 특히 강조되는데요. 손씻기에 필수품이 있다면 바로 비누와 각종 세정제를 들 수 있습니다. 물체 표면의 이물질을 말끔하게 없애는 비누와 세척제에 숨겨진 화학 원리를 살펴봅니다.

비누의 원료, 트라이글리세라이드
미끌미끌한 비누는 트라이글리세라이드라는 물질을 원료로 사용하여 만들어집니다. 트라이글리세라이드(triglyceride)는 지방과 기름을 구성하는 물질로, 쉽게 말해 지방이라고 할 수 있습니다. 보다 화학적으로 표현하자면 지방산 3개를 가진 글리세롤입니다. 지방산은 탄소 원자들이 일렬로 결합된 탄소 사슬(R) 말단에 카복실기(-COOH)를 가진 물질입니다. 이들 지방산 3개가 글리세롤 분자 하나와 결합하여 생성됩니다. 트라이글리세라이드는 수산화나트륨이나 염화수소를 촉매로 반응하여 글리세롤과 지방산으로 분리됩니다.
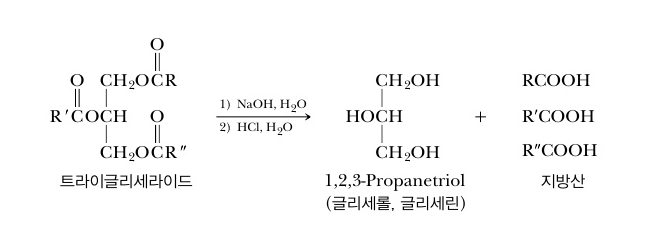
비누의 생성 과정
천연 비누는 우지와 코코넛 기름을 혼합하여 만듭니다. 소의 고체 지방을 증기로 녹이면 층으로 나눠지는데, 그 중 상층의 우지층을 제거합니다. 트라이글리세라이드와 수산화나트륨(NaOH)를 함께 끓이면 비누화 반응이 일어나고, 글리세롤과 나트륨(소듐) 비누로 나눠집니다. 나트륨 비누는 지방산에서 수소가 분리되어 나가고 그 자리를 나트륨(Na)이 채운 형태입니다.
여기에 소금을 첨가하여 침전시킨 후, 물을 제거나 글리세론은 증류법을 이용하여 회수합니다. 가공 전의 비누는 아직 소금, 수산화나트륨 및 여러 불순물을 포함하고 있기에, 몇번의 정제 과정을 거쳐 비누로 탄생시킵니다.
비누가 오염물질을 제거하는 방법
비누는 크게 극성을 띠는 '머리' 부분과 극성을 띠지 않는 '꼬리'부분으로 나눌 수 있습니다. 극성인 머리는 나트륨과 나머지 카복시기 사이의 전자가 카복시기 쪽으로 치우쳐 있기에 전기적 성질, 즉 극성을 띱니다. 탄소 사슬은 전자가 비교적 균일하게 분포하여 전기적 성질을 띠지 않습니다. 물 분자들은 극성을 띠는 머리와 결합하려는 특성이 있어, 물속에서 비누 분자들은 자발적으로 밀집하여 마이셀(micelle)이라는 구조를 형성합니다. 물과 친화성이 낮은 소수성(hydrophobic) 부분이 구의 내부에 자리하고, 물과 친화적인 친수성 부분(hydrophilic)이 구 표면에서 물과 접촉합니다. 한편 전자를 상실한 나트륨은 이온이 되어 물 속을 떠돕니다.

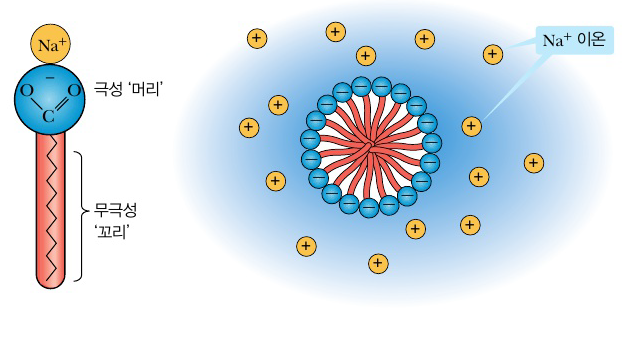
기름, 지방류, 수지와 같은 오염 물질들은 물과는 달리 극성을 띠지 않아 물에 녹지 않습니다. 세탁기 안에서 비누와 오염 물질을 함께 섞으면, 무극성 꼬리 부분이 자신들과 같은 특성인 무극성 오염 물질 분자들에 달라붙어 마이셸을 형성합니다. 이러한 방법으로 오염 물질들이 옷, 손 등 물체에서 잘게 비누에 의해 분리되어 제거되는 것입니다.
합성 세제의 구조
비누의 작용을 연구한 화학자들은 합성 세제를 고안하였습니다. 이들 세제를 구성하는 분자들은 긴 탄소 사슬을 가지고 말단에는 극성을 띠는 다른 기, 예컨대 설폰산 기 (-SO3)를 포함하고 있습니다. 이러한 방식을 취함으로써 카복실기를 가지는 비누와는 다르게 물에 녹지 않는 염이 형성되어 목욕이나 세탁 뒤 광택을 손상시키고 표면을 거칠게 만드는 단점을 막을 수 있었습니다. 합성 세제를 구성하는 대표적인 물질로는 알킬벤젠설폰산이 있습니다. 음이온 세제를 보면, 왼쪽에는 긴 탄소 사슬이 있고 그 뒤를 벤젠 고리가, 말단에는 설폰산 이온 및 나트륨 이온이 부착되어 있습니다. 이러한 유형의 세제는 비누 시장의 90%를 점유한다고 알려져 있습니다.
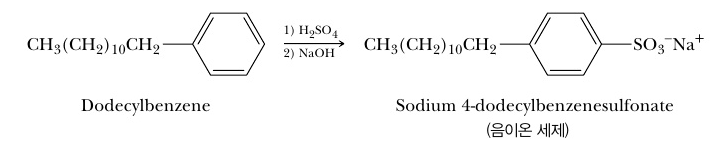

지금까지 천연 비누의 구조와 세척 원리, 그리고 단점을 극복하기 위해 고안된 합성 세제의 구조에 대하여 알아보았습니다. 생활 속 여러 물질들에 화학 원리가 숨겨져 있다는 사실, 기억해 주세요.





